Některé kovy, třeba železo či měď, zná lidstvo od nepaměti. Jiné známe z pohledu historie teprve krátce, ovšem v posledních desetiletích jejich význam stále roste. K těmto kovům patří také nikl a titan. Mohlo by se zdát, že mají pouze okrajové uplatnění, ale opak je pravdou.
Asi těžko bychom hledali civilizovaného člověka, který by s těmito dvěma prvky nepřišel do kontaktu. Pokud používáte zubní pastu nebo opalovací krém, tak jste se téměř jistě setkali s oxidem titaničitým… A věděli jste, že nikl je vlastně nadávka?
Od meteoritů k oceli
Nikl je všudypřítomný stopový prvek. Nacházíme ho v potravinách, velké množství je ho obsaženo v jádru Země, v zemské kůře vytváří například minerály pentlandit (sulfid železa a niklu) nebo millerit (sulfid nikelnatý). Kovový nikl je také důležitou součástí mnoha meteoritů, které právě díky němu dokážeme rozeznat od pozemských hornin.
Tento stříbřitě bílý kov s vysokým leskem objevil roku 1751 švédský chemik a mineralog Cronstedt. Nikl izoloval z minerálu nikelinu (chemicky arsenid niklu), který se vyskytuje i v Krušných horách. Odtud také pochází název prvku. Němečtí horníci totiž tehdy hledali hlavně rudy mědi a nikelin je svojí hnědočervenou barvou velmi připomínal. Přitom z něj ale nebyli schopni žádnou měď vyrobit a toxické sloučeniny arsenu navíc způsobovaly těžké otravy.
Horníci proto začali minerálu říkat Kupfernickel (volně přeloženo „falešná měď“; jde o složeninu z německého Kupfer – měď – a Nickel, což bylo označení zlomyslného podzemního skřítka). Dnešní název nikl je tedy vlastně část historické hornické nadávky.

Historie niklu a jeho slitin je ale mnohem delší. Ještě než se lidé naučili získávat železo z rud, vyráběli různé předměty z meteoritického železa. To se vyznačuje velkou pevností, tažností a odolností proti korozi, což je způsobeno právě přítomností niklu. Díky těmto vlastnostem přetrvaly výrobky z meteoritického železa až do našich dnů. Ze stejných důvodů byla již ve starověké Číně oblíbená slitina mědi, zinku a niklu, takzvaný pakfong.
Rozmach využívání niklu nastal v 19. století, kdy přišla do módy slitina alpaka (nazývaná také nové stříbro nebo čínské stříbro), odpovídající svým složením pakfongu. Z alpaky se vyrábělo nádobí, mince i další předměty denní potřeby.
Nikl se také začal nanášet na povrch železa jako vrstva zabraňující tvorbě rzi. Povrch různých korodujících materiálů, například neodymových magnetů, se niklem pokrývá dodnes. Později se tento prvek začal přidávat do oceli, protože zvyšuje její tvrdost a korozivzdornost. Nejvíce niklu se dnes spotřebuje právě jako přísada do oceli.


Slitiny, baterie a tuky
Další slitiny tohoto kovu vynikají pozoruhodnými vlastnostmi. S mědí tvoří nikl Monelovu slitinu, která má excelentní odolnost proti korozi. Dokonce odolává i nejreaktivnějšímu prvku, fluoru, při jehož výrobě se také používá. Najdete ji však hlavně v zařízeních vystavených silně korozivním přírodním podmínkám, třeba v továrnách na odsolování mořské vody.
Slitina niklu s titanem má elastické vlastnosti a tvarovou paměť: drát z ní vytažený můžete libovolně zohýbat, ale po zahřátí se sám vrátí do původního tvaru. Její aplikace sahají od tryskových pohonů přes lehké a nezničitelné brýlové obroučky až po léčbu infarktových stavů takzvanými stenty, jež rozšiřují zúžené cévy.
Nikl výborně pohlcuje vodík, proto jsou jeho slitiny například s lanthanem a hořčíkem zkoumány jako možná „úložiště“ vodíku pro alternativní pohony. Je také součástí mnohem běžnějších zdrojů energie – známých nabíjecích baterií (přesněji akumulátorů), kde ho najdete v kombinaci s kadmiem nebo jinými kovy.
V potravinářském průmyslu slouží nikl jako katalyzátor reakcí, kterými z rostlinných olejů vznikají ztužené tuky.
Použití niklu v mincích a špercích je omezené. Nemalá část populace je na něj totiž alergická a již krátký kontakt s ním vyvolá u citlivých lidí zánětlivé onemocnění kůže.
Obtížně polapitelný, ale užitečný titan
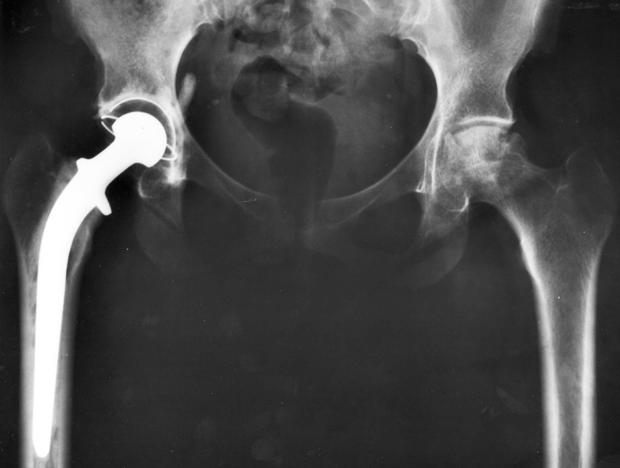
Titan má na rozdíl od niklu skvělou biokompatibilitu, což znamená, že lidské tělo ho dobře snáší a nevytváří proti němu protilátky. Proto se tento kov často využívá v medicíně – například k výrobě umělých kloubních náhrad nebo ke spojování kostí při složitých zlomeninách.
Ačkoliv je titan devátým nejhojnějším prvkem v zemské kůře (je ho zde 70× více než niklu), byl v čistém stavu připraven teprve roku 1910. Jeho výroba je totiž extrémně energeticky a technicky náročná, hlavně kvůli nutnosti používat kovový hořčík. Zpracování titanu prodražuje i to, že se snadno slučuje s kyslíkem, takže je potřeba pracovat v ochranné atmosféře dusíku či argonu.
O existenci titanu jako prvku se nicméně vědělo již od 18. století díky minerálům rutilu (oxid titaničitý, TiO2) a ilmenitu (oxid železnato-titaničitý, FeTiO3). Svůj výstižný název dostal podle Titánů z řecké mytologie, kteří byli uvězněni v zemi.

Kov pro armádu i civilisty
Titan zásadně ovlivnil průběh studené války. V šedesátých letech 20. století umožnil Američanům zkonstruovat špionážní letadlo Lockheed SR-71 Blackbird, které díky němu mohlo létat rychlostí překračující trojnásobek rychlosti zvuku a dosahovat výšek přes 25 kilometrů. To byly ve své době až neuvěřitelné parametry.
Aby letadlo dokázalo vzlétnout tak vysoko a letět tak rychle, bylo potřeba použít právě titan, protože je asi dvakrát lehčí než ocel a dvakrát pevnější než hliník. Navíc odolává vysokým teplotám i korozi.
Blackbird byl zajímavý mimo jiné i tím, že se při letu vysokou rychlostí velmi zahříval kvůli tření vzduchu (až k 500 °C). Jelikož se materiály teplem roztahují, bylo nutné na trupu a křídlech letadla ponechat mezery, odborně řečeno dilatační spáry. Na zemi ovšem těmito mezerami unikaly pohonné hmoty, takže letadlo muselo tankovat ve vzduchu. Jakmile se ale vzneslo a dosáhlo určité rychlosti, kov se zahřál, roztáhl a konstrukce perfektně těsnila.
Letoun byl kvůli použití titanu velice drahý. USA ani neměly dostatečně velké zásoby tohoto kovu, a tak se jeho dodavatelem paradoxně stal Sovětský svaz – samozřejmě aniž by tušil, na co ho Američané potřebují. Sovětské území přitom bylo jedním z hlavních cílů špionážních letů Blackbirdu.

Titan a jeho sloučeniny mají obrovský význam i dnes. Kovový se uplatňuje ve vesmírném programu, ve vojenských aplikacích nebo ve slitinách pro jízdní kola, tenisové rakety, golfové hole a jiné profesionální sportovní nářadí.
Přes 90 % produkce titanu ovšem slouží lidstvu ve formě oxidu titaničitého (TiO2). Ten se používá jako bílý pigment – takzvaná titanová běloba – při výrobě malířských nátěrů, ale i zubních past, papíru či některých potravin, například mléčných výrobků. Oxid titaničitý najdete také v kosmetice, přesněji v opalovacích krémech. Tvoří totiž jejich účinnou složku, která pohlcuje nebezpečné ultrafialové záření.






























































