Látky schopné rychle uvolnit velké množství energie označujeme jako energetické materiály. Tento pojem je téměř synonymem libozvučného českého výrazu „výbušnina“. Energetické materiály si spojujeme hlavně s armádou či terorismem. Není to úplně nezasloužená pověst, většinu jich ale spotřebují civilisté. Výbušniny pomáhají těžit nerosty, bouráme s nimi nepotřebné stavby a díky takzvaným propelentům dokážeme vynášet na oběžnou dráhu komunikační i jiné družice. Neměli bychom zapomínat ani na zábavnou pyrotechniku. S energetickými materiály se zkrátka setkáváme dosti často.
Rozhodují rychlost a kyslík
Poněkud překvapivě se z těchto materiálů neuvolňuje žádné závratné množství energie. Třeba při výbuchu 1 kg hexogenu (RDX) se ve formě tepla uvolní 5 036 kJ. Pro porovnání: konzumací 1 kg chleba získáme asi 10 000 kJ a spálením 1 kg černého uhlí dokonce 27 000 kJ.
Chleba přesto není moc běžně používanou výbušninou. Ne že by však armáda měla takovou úctu k božímu daru – potíž je, že energie se z chleba uvolňuje strašlivě pomalu. Při výbuchu (explozi, detonaci) probíhá chemická reakce takřka bleskově. Ve výbušnině se šíří rychlostmi řádově kilometrů za sekundu, tedy rychleji než zvuk. V případě podzvukového šíření reakce (řádově metry za sekundu) mluvíme o deflagraci a „obyčejné“ hoření postupuje jen o milimetry až centimetry za sekundu.
Chleba a výbušniny mají nicméně leccos společného. Podobně jako škroby a cukry v chlebu jsou i výbušniny nabity energií chemických vazeb, která se uvolňuje v průběhu oxidace. Při trávení chleba získáváme energii z cukrů oxidací vzdušným kyslíkem. Molekuly kyslíku jsou ve vzduchu hrozně daleko od sebe, a nelze se tedy divit, že k uvolnění energie nedojde rychle. Výbušnina proto musí najít kyslík přímo v sobě, ve vlastních molekulách. Základním palivem klasických výbušnin je – stejně jako u cukrů – uhlík a vodík. Protože se kyslík do řady organických molekul dobře zavádí v podobě takzvaných nitroskupin (–NO2), obsahují výbušniny obvykle i dusík. Uhlík a vodík se při explozi spalují ideálně až na oxid uhličitý a vodu.

Chemie explozí
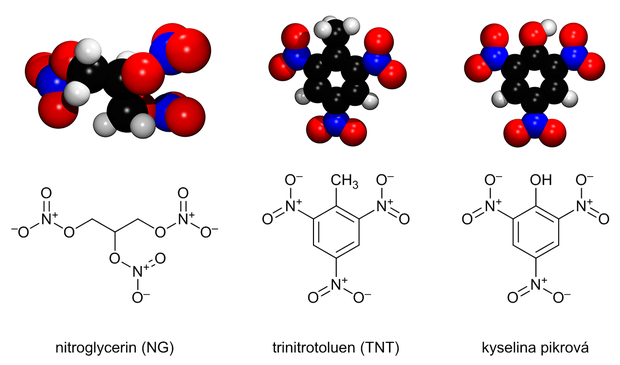
Pojďme se podívat, jak vypadají některé běžné výbušniny. Obrázek níže ukazuje strukturní vzorce třech „tradičních“ výbušnin: nitroglycerinu, trinitrotoluenu (TNT) a kyseliny pikrové. Molekuly mají vždy uhlíkový skelet, na který je navěšena řada nitroskupin. Pokud by se skelet úplně oxidoval na oxid uhličitý a vodu, navázal by na sebe každý atom uhlíku dva atomy kyslíku a na každé dva vodíky by se navázal jeden kyslík. Většina výbušnin ovšem tolik kyslíku nemá. Například TNT se sumárním vzorcem C7H5N3O6 by potřeboval ke kompletní oxidaci 16,5 atomu kyslíku, v molekule jich však má jen šest.
Míru nedostatku kyslíku vyjadřujeme veličinou nazývanou kyslíková bilance. Dá se vypočítat ze sumárního vzorce sloučeniny (ten udává počet atomů jednotlivých prvků v molekule, obecně CaHbNcOd) podle jednoduché rovnice:
kyslíková bilance = [(d − 2a − b / 2) × 16 / M] × 100 %,
kde číslo 16 reprezentuje atomovou hmotnost kyslíku a M je molární hmotnost sloučeniny. Záporná hodnota kyslíkové bilance znamená, že se v molekule nedostává kyslíku k úplnému spálení na oxid uhličitý a vodu. Kladná bilance by naopak značila, že molekula má kyslíku přebytek.
Pro TNT má tato veličina hodnotu −74 %, pro hexogen (C3H6N6O6) −21,6 %. Protože energetickým sloučeninám se při výbuchu nedostává kyslíku, uvolní se z nich méně energie než při pomalém, ale důkladném trávení chleba za přístupu kyslíku z vnějšího prostředí.
Na ideální spálení za vzniku pouze oxidu uhličitého a vody nám chybí kyslík, takže jaké další látky se vlastně během exploze tvoří? V různé míře jsou to saze, oxid uhelnatý, vodík, dusík, oxidy dusíku nebo třeba amoniak. Díky fyzikální chemii dokážeme produkty výbuchu předpovědět. Už za druhé světové války formuloval americký chemik ukrajinského původu George Kistiakowsky sadu jednoduchých pravidel (Kistiakowského–Wilsonova pravidla), která poskytují alespoň odhad detonačních produktů:
• Uhlík se oxiduje na oxid uhelnatý.
• Pokud ještě zbývá kyslík, oxiduje se vodík na vodu.
• Pokud stále zbývá kyslík, oxid uhelnatý se oxiduje na oxid uhličitý.
• Dusík se uvolňuje jako dvouatomové molekuly N2.
Pro hexogen tak například vychází tato reakce:
C3H6N6O6 → 3 CO + 3 H2O + 3 N2.

Hledání ideální výbušniny
Jakmile víme, které produkty vznikají, můžeme s pomocí chemické termodynamiky snadno vypočítat teplo uvolněné během detonace. Uvolněná energie je však jenom jedním z kritérií, která jsou důležitá při navrhování energetických materiálů. Podstatné je také množství vznikajících plynů (čím více plynných molekul se vytvoří, tím lépe výbušnina něco roztrhá), hustota výbušniny či detonační rychlost. Vyšší hodnoty těchto parametrů znamenají větší fragmentační účinek výbušniny neboli její brizanci.
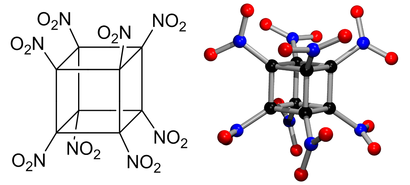
Fyzikálně-chemické modelování umožnuje navrhnout „ideální výbušninu“. Takovou vysněnou sloučeninou byl třeba oktanitrokuban (ONC), u něhož byla předpovězena velká hustota a detonační rychlost převyšující 10 km za sekundu – což je skoro 30× více než rychlost zvuku. Molekula byla v roce 2000 skutečně připravena, a to komplikovanou mnohastupňovou syntézou. Ukázalo se ovšem, že optimistická očekávání tak docela nesplňuje.
Skvělá výbušnina musí mít i další dobré vlastnosti. Především by neměla být drahá. Kupříkladu oktanitrokuban je dražší než zlato, přičemž je ale daleko méně stabilní. Výbušnina by také neměla být příliš citlivá na vnější podněty, aby manipulace s ní byla bezpečná. Bohužel jde výkonnost výbušniny často ruku v ruce s velkou citlivostí.
Od střelného prachu k Semtexu
Nejstarším energetickým materiálem je střelný prach – směs dřevěného uhlí, síry a dusičnanu draselného. Počátky historie střelného prachu jsou stále zahaleny tajemstvím. Nicméně se zdá být pravděpodobné, že už v 9. století byl používán v Číně a do Evropy se dostal někdy ve 13. století. Teprve zde začal sloužit vojenským účelům. Potřebný dusičnan se získával „biotechnologicky“, z rozkládajícího se organického materiálu. Bylo kolem toho hodně zápachu, takže výrobny dusičnanu neboli sanytrovny neviděli obyvatelé ve svých městech rádi. V Praze se jeden takový podnik nacházel na nynější ulici 17. listopadu.
Rozvoj výbušnin nastal v 19. století. Roku 1846 syntetizoval italský profesor Ascanio Sobrero nitroglycerin a brzy zjistil jeho explozivní povahu. Immanuel Nobel, otec známého Alfreda Nobela, vybudoval v roce 1863 malou továrnu na výrobu nitroglycerinu, která však byla již v roce 1864 zničena výbuchem. Při tomto neštěstí také zahynul Immanuelův nejmladší syn Emil. Po dalším výbuchu v roce 1866 se Alfred Nobel zaměřil na otázky bezpečnosti a vytvořil z nitrocelulózy a nitroglycerinu relativně bezpečný želatinový dynamit. Střelný prach byl během 19. století v armádách postupně nahrazován kyselinou pikrovou. Ke konci století začal být vyráběn a ve vojenství používán také trinitrotoluen, který se stal dominantní výbušninou první světové války.
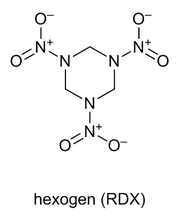
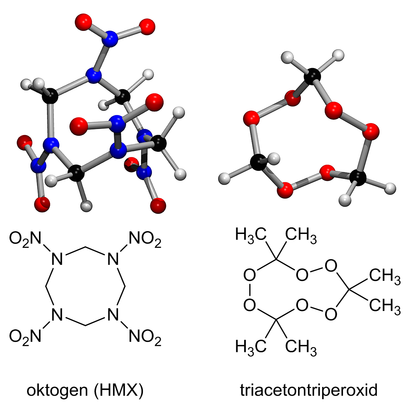
Za druhé světové války a po jejím ukončení se výrazně prosadily látky RDX (Royal Demolition eXplosive, hexogen) a HMX (Her Majesty's eXplosive, High Melting point eXplosive, oktogen). Po válce začaly být výbušniny zabudovávány do polymerů a byly tak vytvořeny plastické trhaviny. Příkladem může být SEMTEX ze Semtína u Pardubic, vyráběný od roku 1964. Jinou skupinou výbušnin jsou látky založené na přítomnosti peroxidické vazby. Známou a velmi nevyzpytatelnou sloučeninou tohoto druhu je triacetontriperoxid – dnes asi nejčastější amatérská výbušnina, která se používá i při teroristických útocích.
Současné trendy
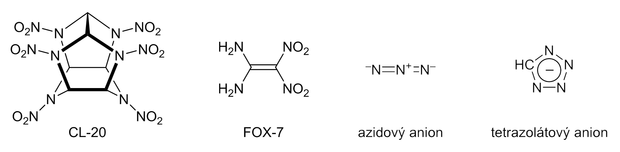
Od konce studené války se obnovil výzkumný zájem o nové energetické materiály. Zrodila se řada nových výbušnin s potenciálně zajímavými vlastnostmi. Příkladem je látka nazvaná CL-20. Jde o sloučeninu s nejvyšším obsahem energie a také s nejvyšší hustotou mezi organickými látkami. Cena je zatím poněkud vysoká – v roce 2012 činila asi 1 300 amerických dolarů za 1 kg oproti 100 dolarům za 1 kg HMX. Jinou uvažovanou energetickou sloučeninou je už zmíněný oktanitrokuban. V roce 1998 se objevila látka FOX-7, která je zhruba stejně výkonná jako RDX, ovšem výrazně méně citlivá. Cena však zatím opět nehraje v její prospěch.
Mnoho úsilí bylo věnováno energetickým materiálům s vysokým obsahem dusíku. Energie se zde neuvolňuje oxidací uhlíkové kostry, ale přímo z energeticky bohatých chemických vazeb v molekule sloučeniny. Tyto látky vytvářejí téměř výhradně plynné zplodiny, při explozi tedy nevzniká dým. To je výhodné jak z hlediska životního prostředí, tak z hlediska technického (pro využití k pohonu raket). Z dusíkatých energetických sloučenin se již dlouho setkáváme s azidy, které najdeme například v automobilovém airbagu. Rovněž se začínají používat takzvané tetrazoláty.
Ilustrační foto nahoře: Zapálený balónek naplněný vodíkem. Nejedná se o explozi v pravém smyslu slova, neboť v balónku nebyl přítomen žádný kyslík – vodík tak jen velmi rychle shořel při kontaktu s okolním vzduchem. Foto: Petr Jan Juračka.
































































